- 2019.06.27
- コラム
「基礎臨床一体型」で治療法を開発する-iPS細胞を用いた神経変性疾患の治療を目指して
ASCA Bulletin 22号では、慶應義塾大学医学部生理学教室教授の岡野栄之先生を取材させていただきました。
京都大学山中伸弥教授らによるiPS細胞技術の確立以降、日本では2013年の滲出型加齢黄斑変性に対する自家iPS細胞由来網膜色素上皮細胞シートを移植する臨床試験を皮切りに、2018年前半にはパーキンソン病及び虚血性心筋症の患者を対象としたiPS細胞を用いた臨床試験が承認。そして2018年末には筋萎縮性側索硬化症(ALS)を対象としたiPS細胞創薬に基づいた医師主導治験が承認されました。翌年2月には亜急性期脊髄損傷の臨床試験の実施が承認されましたが、岡野先生は、これら2つの画期的な治験を主導されておられます。
分子神経生物学・発生学分野の研究者を目指した経緯
高校生の頃は物理学に興味がありましたが、エルヴィン・シュレーティンガーのようなノーベル賞を受賞した高名な物理学者の多くが生命科学に興味を持っていたことから、今後は生命科学が非常にエキサイティングな学問分野になると考え、生命科学や医学の研究をするために医学部に入学。医学部在学中に、物理化学的手法を用いて生命科学を研究したいと考えて分子生物学を学び、分子生物学的手法を用いたがん研究に興味を持ちました。ただ、大学を卒業する頃には多数の研究者ががん遺伝子の研究を行うようになり、研究者としてこの分野に参入し、成果を上げていくのは厳しいと考えました。
一方、神経分野では、形態学的な研究や電気生理学的な研究は行われていたものの、分子生物学的手法を用いた研究はほとんどなく、脊髄損傷を含む神経系の疾患のほとんどで治療法が全くない状況でした。そこで、神経系の理解に分子生物学的な手法を取り入れることにより、疾患原理を解明し、治療法を見つけることができるのではと考え、神経系の発生を分子生物学だけでなく、幹細胞生物学の観点からもアプローチするようになったのです。
脊髄損傷の治療法開発までの道のり
米国ジョンズ・ホプキンス大学に留学した頃(1989年)には、神経の発生異常を示すさまざまな変異体を同定し、神経発生にかかわる重要な遺伝子を同定する研究を開始し、ショウジョウバエにおいてMusashiというRNA結合タンパク質を発見しました。当初このMusashiタンパク質は、ショウジョウバエの感覚器発生に関与するタンパク質として同定されましたが、その後、哺乳類では神経幹細胞に強く発現しており、成人の脳にも神経幹細胞が存在することが分かりました。世界で初めてヒトの神経幹細胞の存在を示す論文を発表して以来、基礎生物学的な研究から臨床応用可能な研究へと変化し、注目を浴びるようになりました。
臨床研究に立ちはだかった障壁
この論文の発表に至るまでに、ショウジョウバエだけでなくマウスにもMusashiタンパク質が保存されていることが分かっていたため、当然ヒトに存在していても不思議ではなかったのですが、このヒトでの論文の反響があまりにも大きく、マウスとヒトにおける研究成果に対する世間の捉え方はこんなにも違うものなのかと大変驚きました。この論文を発表した1998年より、脊髄損傷に関する研究を始め、2001年に慶応義塾大学に戻った際に整形外科と共同チームをつくり、本格的に臨床を目指した基礎研究を開始しました。2002年にはサルの脊髄損傷モデルを作製し、サルモデルにヒトの胎児由来の神経幹細胞を移植することにより運動機能の回復に成功しました。この研究はワシントンポストをはじめとする海外メディアで大きく取り上げられ、世界的に注目を集めました。通常であれば、この動物モデルでのデータを用いて臨床に応用するというステップに移行するのですが、日本では倫理的なハードルが非常に高く、2006年に厚生科学審議会により、倫理的観点からヒトのES細胞由来や胎児由来の細胞を用いた臨床研究ができなくなってしまいました。
iPS細胞の登場
しかし、2006年に京都大学の山中伸弥教授により開発されたiPS細胞技術がこの困難な状況を打破するきっかけとなりました。このiPS細胞技術により胎児由来細胞やES細胞を使わずに神経幹細胞を大量に作製することが可能になりました。山中教授と共同研究を行い、2010年にはマウスのiPS細胞を使いマウスの脊髄損傷モデルの機能回復に成功した論文を発表し、2012年にはヒトのiPS細胞由来の神経幹細胞でサルの脊髄損傷モデルを治すという論文を立て続けに発表しました。これらの脊髄損傷モデルに移植したiPS細胞由来の神経幹細胞は、神経細胞やグリア細胞(オリゴデンドロサイト)に分化していることが分かりました。脊髄損傷では、外傷による機械的な損傷(一次損傷)に引き続き起こる二次損傷の1つとして、神経細胞の軸索を取り囲む髄鞘を形成するグリア細胞のアポトーシスにより脱髄という現象を起こすことが知られています。髄鞘は絶縁体として働いているため、脱髄が進行すると神経の伝導速度が低下し、運動機能が低下する原因となります。このため、脊髄損傷モデルでは、移植したiPS細胞由来の神経幹細胞がオリゴデンドロサイトに分化し再髄鞘化した結果、運動機能が回復したと考えています。これらの成果をふまえ、2013年よりヒトへの応用を目指して、臨床で使えるグレードの神経幹細胞の作製に着手しました。サルモデルでは、レトロウイルスベクターを用いた第1世代のiPS細胞だったため、臨床では使用することができません。また、患者自身の細胞からのiPS細胞を用いる場合、iPS細胞の樹立に3ヵ月、神経分化に3ヵ月と膨大な時間がかかってしまいます。脊髄損傷後1ヵ月程度の亜急性期に神経幹細胞を移植するのが最も効果的なことがわかっていたことから、臨床用にすぐ使えるiPS細胞バンクを作り、移植可能な高品質の神経幹細胞を作製・冷凍保存しておき、いつでも亜急性期の患者さんに投与できるよう準備することにしました。
臨床研究での規制上、動物由来の物質を含む培地は使用できないため、臨床グレードの材料を用いてヒトのiPS細胞から神経幹細胞を分化誘導する培養系を確立する必要がありました。まず、いくつかの方法で培養した細胞をマウスの脊椎損傷部や脳に移植し、腫瘍を形成せず、移植部位で分化増殖する培養方法を選択しました。さらに、分化誘導の途中で確認試験や純度試験を実施し、すべての試験で判定基準を満たした細胞のみを選別しました。その結果、未分化iPS細胞が10万個中1個未満という水準が得られる培養方法を確立しました。神経前駆細胞を200万個移植する場合、未分化iPS細胞は20個未満となりますが、この数では腫瘍を形成しないことが別の非臨床試験において確認済みです。この培養系を確立するのに5年を要し、ようやく昨年の2018年11月末にヒトiPS細胞を用いた臨床研究の承認を得ることができました。この臨床研究では、脊髄損傷になって2~4週間という亜急性期の患者さんが対象となります。残念ながら、既に脊髄損傷となっている慢性期の患者さんは対象外です。しかし、細胞間の情報伝達経路の1つであるNotchシグナルが働かないようにして神経幹/前駆細胞を前処理すると、ニューロンへ分化するだけでなく、軸索の再生を促進することが分かりました。そこで、これまで細胞移植単独では治療効果を得ることができなかった慢性期の脊髄損傷モデルマウスに対し、γセクレテーゼ阻害剤(Notchシグナル阻害剤)で前処理したヒトiPS細胞から樹立した神経幹/前駆細胞を移植することにより、軸索の再生と伸長に加え、再髄鞘化も誘導され、運動機能を回復・維持させることに成功しました。この成果をもとに、2~3年後には、慢性期の脊髄損傷患者を対象とした臨床研究を開始できるように準備していきたいと思っています。
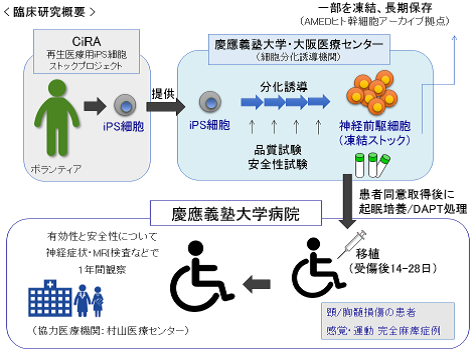
(https://www.keio.ac.jp/ja/press-releases/files/2018/11/29/181128-1.pdf)
iPS細胞を用いた創薬-筋萎縮性側索硬化症(ALS)に効果のある既承認薬剤の同定
ALSに関しては、ALS患者由来のiPS細胞を作製し、神経系の細胞へ分化誘導させることによって、病態を解析し、病態を改善する薬剤の開発を目指した研究を現在行っています。ALSは筋肉を支配する運動ニューロンが変性して脱落することにより、随意筋が麻痺し、進行すると人工呼吸器を装着しなければ生きていけなくなる難病です。ALSの約10%が家族性で、残り90%が孤発性といわれており、家族性については25種類以上の原因遺伝子が特定されています。原因遺伝子の1つであるFUSに変異を有するALS6型の患者さん由来の組織から樹立したiPS細胞を、ALSで選択的に脱落されるとする運動ニューロンへと分化させたところ、原因遺伝子産物であるRNA結合タンパク質(FUS)が本来局在すべき核内から細胞質へと局在異常が生じ、細胞質中にてストレス顆粒という凝集体を形成し、運動ニューロンが死滅するというALS関連表現型をin vitroで示すことが分かりました。また、別の原因遺伝子TARDBPに変異を有し、その遺伝子産物がFUSと同じRNA結合タンパク質の1つ(TDP-43)であるALS10型の患者さん由来のiPS細胞から誘導した運動ニューロンでも、同様のALS関連表現型が起きることが確認されました。このように、in vitroでALSの病態(神経突起の退縮、ストレス顆粒の形成、運動ニューロン死)を再現することが可能となったことから、ALSの病態を改善する薬剤のスクリーニングを実施することにしました。慶應義塾大学の既存薬ライブラリー(約1,500種の化合物)を利用し、その中からALSに対する薬効を持つ薬剤をALS6型及びALS10型患者由来のiPS細胞を用いたアッセイにより選別しました。1,232種類の薬剤をスクリーニングし、ALSに効く可能性のある9つの薬剤を同定しました。その中で最も効果があり、血液-脳関門を通過することが示され、かつ神経の他の疾患に対して適応がある2つの薬剤を特定しました。
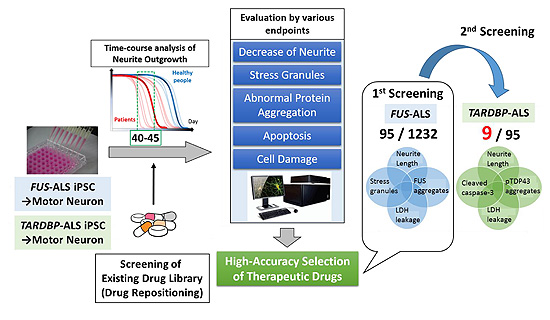
(http://kompas.hosp.keio.ac.jp/sp/contents/medical_info/science/201811.html)
この2つの薬剤をALSの承認薬であるリルゾールとエダラボンと比較した結果、いずれもALSの病態(神経突起の退縮、ストレス顆粒形成、運動ニューロン死)に対して承認薬よりも数倍高い改善効果があることを確認しました。2つの薬剤のうち最も高い効果を示したのがパーキンソン病の治療薬ロピニロールでした。このロピニロールは、1996年から世界中で広く使用されており、日本でも使用経験が豊富です。この薬剤を治療薬として、ALS患者を対象とした医師主導型の第I/IIa相試験を慶応義塾大学病院にて昨年の12月1日から実施しています(UMIN000034954)。なお、ALS6型及びALS10型の患者さん(SOD-1変異なし)、並びに孤発性ALSの患者さんのうちFUS又はTDP-43蓄積表現型を呈する患者さんにおいてロピニロールの効果が高かったことから、今回の臨床試験ではSOD-1変異の家族歴を有する患者さんやSOD-1変異を過去に診断されたことのある患者さんは対象外となっています。
次世代へのメッセージ
結核は明治時代では死に至る病気でしたが、現代では抗生物質によって治癒可能となっており、死に至る病気ではなくなっています。このように、それぞれの時代で死に至る病気、治らない病気というものが存在しますが、絶えずそういう病気に対して治療法を見出すということにチャレンジしてほしいです。治療法がない病気の場合、多数の患者を診察しても新しい治療法の開発にはつながりません。病気のメカニズムを詳しく掘り下げて研究することが必要です。慶應義塾大学では「基礎臨床一体型」と表現していますが、基礎研究者と臨床医師との共同チームを作って新しい治療法について研究することが非常に大事です。大阪大学医学部教授として赴任した時、当時医学部長だった岸本先生から「あんたは研究も儲かってなんぼのもんやな」と言われたとき「はあ」としか答えられず、何のことかさっぱり分かりませんでした。しかし、最近になってやっとその意味が分かってきました。どんなに優れた治療法を開発しても最終的に患者さんに提供できなければ無意味なのだ、と。保険適用となり保険でカバーされるような薬として企業が販売することができて初めて、新しい治療法を普及させることができるのです。そのためにも、大学だけでなく企業や規制当局とも協働し、場合によっては自分達で会社を設立する必要がでてくるかもしれません。研究者は今後、実験室で研究するだけでなく、これまで以上に社会とのかかわりが重要になってくると思います。また、現在(2019年3月取材時)当研究室では試薬を調製・管理する技官を募集中ですが、応募資格として、コミュケーション能力が高くチームプレーを得意とする人を特に重視しています。治療法の開発という大きな目的を達成するには、コミュニケーションとチームプレーが重要です。
岡野栄之先生
【略歴】
慶應義塾大学医学部卒。慶應義塾大学医学部助手、大阪大学蛋白質研究所助手、米国ジョンズ・ホプキンス大学医学部研究員、東京大学医科学研究所助手、筑波大学基礎医学系教授、大阪大学医学部教授を経て、2001年より慶應義塾大学医学部教授(現職)に至る。
インタビューを終えて
ご苦労を乗り越えらえたエピソードを盛り込もうと、「一番ご苦労なさったことは何ですか」とお聞きしたところ、「いろいろな困難はありましたが、あえて苦労話として語るほどことでもありません」とさらっとお答えくださいました。研究に困難はつきもの。落ち込む時間があったら、次の可能性を探る。短い時間で脊髄損傷とALSという2つの疾患について治療法の糸口にたどり着かれたのは、必ず治療法を見出すという揺るぎない覚悟があるからだと感じました。
インタビュアー:福味 知嘉子
(ASCA Bulletin 23号 2019年6月発行より)
ASCA Bulletinとは:
アスカコーポレーションが年3回発行している広報誌です。ご興味のある方は、弊社営業部までご連絡ください。


