- 2019.03.01
- コラム
iPS細胞を用いた心筋再生医療―重症心不全患者の鼓動を蘇らせる

ASCA Bulletin 21号では、大阪大学大学院医学系研究科 外科学講座 心臓血管外科学教授の澤 芳樹 先生を取材させていただきました。
ヒトiPS細胞の樹立から10年余りが経ち、臨床応用を目指した研究が活発になってきました。その中で、iPS細胞を使用した心筋細胞の再生医療に取り組んでいるのが、臨床・研究両面で世界トップレベルの取り組みを続ける大阪大学医学部 心臓血管外科です。本年5月に重症虚血性心筋症の患者さんを対象にした臨床研究の承認が下りたばかりで、今まさに世界中から注目を集めています。今回は、その研究をリードされる澤芳樹 教授に研究の背景や今後の展望についてお話を伺いました。
心不全の「パンデミック」に立ち向かう
心不全はさまざまな心疾患の最終形態で、世界的には第1位の死因です。がんが多い日本でも増加しています。この増加の原因には、高齢化や生活習慣の欧米化という要因もあるのですが、もうひとつの側面として、急性期の治療が進めば進むほど、慢性期の心不全は増加します。すなわち、急性期の治療で生命は助かるものの、その後に心臓の機能が戻らず、徐々に進行していくというパターンです。こうした背景から、人口減にもかかわらず心不全の患者さんの数は増加し続け、2035年には130万人になると予想されています。心不全のパンデミックとでも呼ぶべき状況にあります。
心不全の初期治療は薬物療法で、その後必要に応じてペースメーカー等のデバイスを用いるのが従来型の治療です。この治療で心機能が維持できたり、心不全が改善されるという状況ならこれらの治療が優先されます。ただ、心不全の難しいところは、こうした治療を受け続けながらも次第に悪化し、再発することです。再発に対して治療すればまた改善するのですが、このアップダウンを繰り返しながら長期的には心機能は下降線をたどり、最終的には人工心臓や心臓移植の適応となります。
世界的には心臓移植が普及しており、例えば米国では年間6,000人の心不全患者さんに対して2,000人ぐらいが心臓移植を受けています。人工心臓は心臓移植の待機のために500人程度、永久使用にも1,000人程度に使用されており、心不全の最終的な治療については米国では医療が充実しています。しかしドナー不足や人工心臓の限界から見ると、本来行うべき心不全治療は十分にはできていません。まして日本の場合は31年遅れて心臓移植を再開し、世界で150番目ぐらいに遅れてスタートしたというのが現状です。私は1999年の脳死移植第1例目から心臓移植に携わっており、ちょうど100例を超えたところです。最近ようやく年間10例を超えるようになりました。しかし、日本で心臓移植の必要な患者さんの数は大体年間1,000~2,000人と言われています。一方で実際に心臓移植が行われるのは年間50例程度で、心臓移植を待機するための人工心臓使用も150~200例に過ぎません。日本の医療は世界のトップクラスで、心臓血管外科においても世界に冠たる成績を出していると言っても過言ではありませんが、心臓移植を実施できる施設が10施設ほどしかなく、その中でも中心的なのは3施設ほどで、年間50例に留まっているというのは、患者さんにとっては大変不幸な状況です。
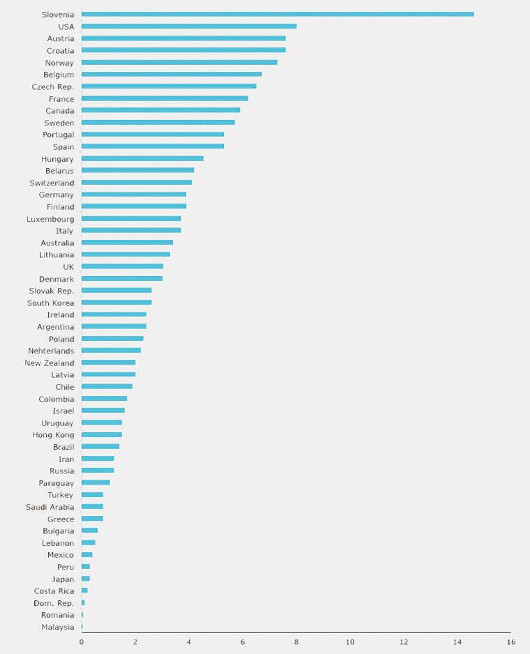
【図1】IRODaT - International Registry on Organ Donation and Transplantation
http://www.irodat.org/img/database/grafics/grafic8.jpg
まだ「再生医療」という言葉はなかった―岡野先生との出会い
私たち心臓血管外科医にとって、このような状況は残念であり、悔しいものです。そこで新しい医療が必要だという発想が出てくるのは自然なことであり、私たちは1990年代後半から心筋細胞を強化する研究に取り組み始めました。当初は遺伝子治療を取り入れようと考えていたのですが、まだ倫理的なハードルが高く、細胞治療に移行していきました。
この頃はまだ、再生医療という言葉はありませんでした。細胞治療の進化によって、私たちの研究の後から言葉が追いついてきたのです。受精卵から胚性幹細胞(ES細胞)が樹立されたのが1998年。その頃には心臓外科の領域でも、フランスのMenaschéらが注入による筋芽細胞での治療を始め、心機能の改善効果があるとして注目を集めていました。その後、100例規模の心筋梗塞後の患者さんに対し自己骨格筋芽細胞移植を行う臨床試験(MAGIC trial)が鳴り物入りで実施されたのですが、これは残念ながらプラセボに対して有意差を示すことができませんでした(1)。
東京女子医科大学の岡野光夫先生にお会いしたのは、2000年の日本人工臓器学会(三重県四日市市)でのことでした(2)。私たちは細胞を注入する実験を行っていたので、シートにするという発想に驚かされ、発表されていた清水達也先生が壇上から下りてくるのをすぐにつかまえて、共同研究を持ちかけました。岡野先生にとっても、臨床サイドからのアプローチは初めてだったので、すぐに意気投合して一緒にやろうということになりました。当時はヒヨコの細胞でin vitroで実験されていたのですが、私たちが培養技術を持っていたラット心筋細胞に、岡野先生に提供していただいたシートを移植してみると非常に効果があることがわかりました。それからin vivoでの実験に進めることができ、使用する細胞も大腿部の筋肉の細胞が良いことがわかって、2004年ぐらいから本格的に再生医療による取り組みが始まりました。
テルモ株式会社との連携が始まったのもちょうどその頃です。彼らも筋芽細胞の培養方法を海外から導入しようとしていたのですが、私たちがやっている実験を試したところ非常に有望な方法だということを知ったそうです。そこで同社自らがGLPレベルでエビデンスを出し、不整脈を起こさず機能改善するということを見出してから私たちへの協力を持ちかけてくれたので、共同研究を行うことになりました。
臨床研究は2007年にスタートしました。この頃になると再生医療に対する期待は非常に高くなっており、研究費が増額された時期でもあったので、症例数は30例前後に及びました。いわば駆け込み寺のように、状態の厳しい方も受け入れましたが、中には社会復帰される方もいました。そしてその経験を踏まえて、テルモ社の治験が開始されたのが2012年です。再生医療推進法など法整備の後押しもあり、2015年には自己骨格筋由来細胞シートとして条件付き承認を得ることができ、2016年6月から実際に保険診療が開始されました。この細胞シートは「ハートシート」と名付けられました。患者さん自身の細胞ですので安全性が高く、また培養方法も比較的シンプルなため、海外からも注目されています。
iPS細胞を用いた細胞シートの開発―山中伸弥先生との出会い
ハートシートの普及にも期待しているのですが、私たちにとってこれはファーストステップです。2007年に私たちがfirst in humanを行ったと同じタイミングで、京都大学iPS細胞研究所(CiRA)の山中伸弥先生がヒトのiPS細胞を樹立されました。そこで、2008年1月からiPS細胞を用いた細胞シートの共同研究をスタートしました。
当初、ヒトの細胞はなかなか心筋細胞にならず苦労しましたが、2012年にProof of Conceptの形で、ヒトのiPS細胞でブタの心機能が改善することを世界で最初に証明しました。その年の秋に山中先生がノーベル賞を取られ、そこから研究のステージが一段上がりました。文部科学省の再生医療実現拠点ネットワークプログラムが設置する疾患・組織別実用化研究拠点(拠点A)のうち、大阪大学は心筋再生治療創成拠点に指定され、2013年から10年間の事業を進めています(図2)。
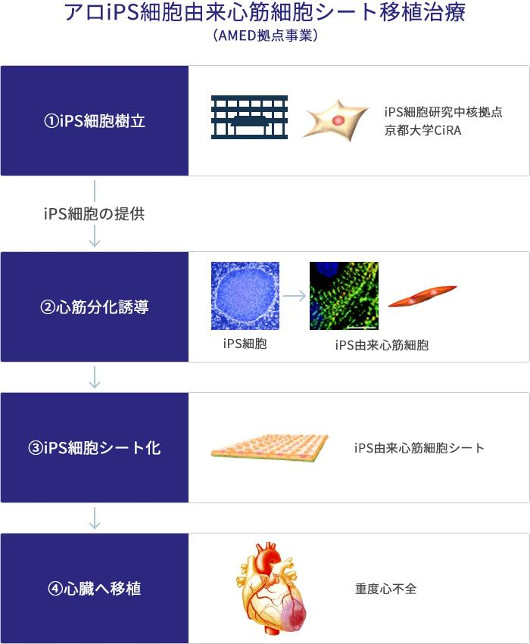
図2. iPS細胞の作製と治療の流れ© 大阪大学 心臓血管外科
http://www2.med.osaka-u.ac.jp/surg1/technology/regenerative-medicine/
なぜiPS細胞を使うのか。ハートシートとは何が違うのか。ひとつの理由は細胞が出すサイトカインの違いです。細胞シートで使用する細胞に求めているのは、それ自体に機能性を持たせるということよりも、細胞増殖を促す作用(trophic effect)です。ハートシートで用いる大腿部の筋芽細胞が分泌するサイトカインは、あくまで足を修復するためのものです。それはそれで有効なのですが、次のステップとしてここからのプラスアルファを考えたときに、やはり心筋細胞のためのサイトカインを出す細胞がほしい。また、動物実験では、細胞が拍動性を持っていることが有効性に影響することもわかっています。これらのことから、多分化能を持つiPS細胞の方が望ましいのではないかということです。
仮に筋芽細胞とiPS細胞の有効性が同等であったとしても、iPS細胞にはリーズナブルであるというメリットがあります。今回使用するiPS細胞は他家由来のものですので、安全性の高さが確立された細胞を、レディメイドで必要なときすぐに使用できます。ただ、これは単に経済的、時間的合理性のみのことを言っているのではありません。ハートシートのように自己由来の細胞を使う場合、細胞を採取するために患者さんに1回多くメスを入れなければいけません。治療の侵襲性を少なくするという点では、このことも無視できない要素だと考えています。
一方で研究のハードルも非常に高くなっています。私たちにとって最も大きな課題は、iPS細胞の腫瘍化をどう克服するかということです。私たちの研究ではiPS細胞を約1億個使用します。これは京都大学など他のiPS細胞の臨床研究よりもはるかに多い数です。このように細胞数が多いと、その中から腫瘍化する細胞をどのように見つけるかということが問題になります。つまり、細胞数が10万個くらいのオーダーであれば腫瘍細胞をゼロにするところまで検出できるのですが、私たちの場合はそこから3桁上がりますので、現代の技術による検出限界を超えているのです。その問題をどう技術的に克服するかを考えなければいけません。
もうひとつは免疫抑制剤をどう使うかという問題です。前述の通り他家由来のiPS細胞を使用しますので、患者さんには免疫抑制剤を服用していただく必要があります。ただ、患者さんの経済負担や合併症のことを考えると、一定の期間にとどめたい。動物実験での比較では、3ヵ月の時点で免疫抑制剤の投与をやめても心機能は落ちないことがわかっています。また一方で、ヒトで筋芽細胞を使用してきた経験でも、この3ヵ月程度で、患者さん自身の細胞であるのにかかわらずやはり細胞は消えていきます。これらのことは、自然免疫の克服の難しさを表していると同時に、免疫抑制剤は使い続けても使用を中止しても同じ結果になるのではないかという可能性を示しています。この考えにはまた別の根拠もあり、確実に腫瘍化するiPS細胞を用いて調べたところ、免疫抑制剤を中止した場合には細胞は腫瘍化せず生着するのですが、免疫抑制剤を使い続けると腫瘍が大きくなり、死に至ります。つまり免疫の抑制を止めることによって、自己の免疫力が戻って腫瘍化を抑えているということになります。現段階で最も安全性に、しかも臨床的な意義を考えて治療することを考えると、免疫抑制剤は3ヵ月に留めるのがリーズナブルだろうと考えていますが、この知見を実際にヒトの研究の中でどう実証していくかは難しい問題です。
患者ファーストで新治療法を届ける
私たちの研究はこのたび国の承認を得て、臨床研究としてスタートしました。ただ、すぐに患者さんに使用できるのかというとそうではありません。まず細胞を新たに作るところから始めなければならず、動物での再検証や腫瘍化の確認などを含め、このプロセスで8ヵ月ほどかかります。また、不幸なことに7月に大阪北部で起こった地震のために、私たちのCPCも被害を受けてしまいました。この被害で振り出しに戻ってしまったので、3ヵ月から半年ほどの遅れが出てしまっています。
このように苦難の連続と言ってもよい状況ですが、しかしこれくらいのことは乗り越えて、一刻も早く患者さんに新しい細胞シートを届けられるように努めています。私たちはまず何よりも医師であり、患者ファーストの考え方が優先されます。心不全の方がどんどん増えていて打つ手がない、この日本のあまりに立ち遅れた状況を打開するためにという使命感を持って研究を進めています。
一方で、この研究は拙速に進められることでもないのです。患者さんの安全性をないがしろにはできないからです。ひとくちに安全にと言っても、これまで助からなかった方の生命を救う最先端の医療を開発しながら、安全性を確保するというのは容易なことではありません。そのためには臨床医学だけではなく、免疫学、腫瘍学なども含め、科学の粋を結集する必要があります。実際には科学が医療のニーズを満たせていないと感じることも多々あるのですが、その葛藤を補うための努力や工夫を続けてハードルを越えていくことが重要です。
その意味では、私たちは良いパートナーに恵まれました。CiRAの山中先生とは、私たちの持っている患者ファーストという理念や、ベストの医療を届けたいという気持ちが共有されていて、一度も議論したことがないほどです。東京女子医科大学の岡野先生も、自施設の心臓外科よりも大阪にある私たちの研究室の方が距離が近いとおっしゃってくれました。研究は人間関係も重要ですから、このように志が共有されていることは心強いと感じます。
また、研究と並行して、患者さん一人ひとりに最適な治療を行っていくことも決して疎かにはできません。私たちのもとには、日本中だけでなく海外からも再生医療を希望する患者さんが訪れます。その中には、状態が厳しくて打つ手が無いような方もおられます。しかし、頼りにされたらそれに応えないといけないのが医師ではないかと思うのです。応える力を持つためには、自分たちで研究開発をしながら、日頃から心不全の患者さんを診て、治療の結果をすぐフィードバックする。そして一人ひとりの患者選択や適応を一生懸命考える。それを繰り返していき、いわば臨床力を高めていくしかありません。幸いにして私たちの研究室には、日本全国から有望で意欲のある若手も集まってきてくれているので、彼らの成長にも期待しながら、医療と研究を両立して進めていきたいと考えています。
若手へのメッセージ
今もっとも重要だと考えているのは人材育成です。日本の医師数は増加していますが、その中で外科医だけが減少しており、3割程度減っていると言われています。まだ顕在化はしていませんが、外科医を普通の手術ができるようになるまで育てるのに20年かかることを考えると、今から真剣に考えておかなければいけない問題です。
私は若い医師には、いつも10年先を見ろと言っています。私自身、心臓外科医として10年先にはどれだけ治療が進化しているかということを常に考えてきました。例えば当科でカテーテル弁置換術をいち早く導入したのもその結果です。現在でもロボット手術など新しい技術をどう取り入れるか。イメージするのが難しければ身近に10歳年上で目標になる先輩がいるか。10年先を考えることができれば、そこから逆算すると今日1日でやるべきことが見えてきます。その積み重ねこそがリアルな成長になると考えています。
(1) Circulation. 2008 Mar 4;117(9):1189-200.
(2) 人工臓器 2000 29(3Supplement): s91
澤芳樹先生
【略歴】
大阪大学医学部卒。フンボルト財団奨学生としてドイツMax-Planck研究所心臓生理学部門、心臓外科部門に留学。帰国後は大阪大学医学部を拠点に心臓外科手術の発展に努める。現在、大阪大学医学部教授、一般社団法人日本再生医療学会 理事長、京都大学 iPS細胞研究所科学アドバイザー など。
インタビューを終えて
澤先生には組織マネジメントにも通じるお話をお伺いすることができました。その中でも印象的だったのが、「リスクを共有する」ということです。例えば、毎日の朝の回診のときに、問題点をその場で分析して共有する。そしてミスや失敗がその原因であれば、ちゃんとリカバリーをして、皆が二度と同じことをしないように徹底する、という取り組みをされているそうです。その積み重ねが研究室全体のlearning curveの底上げに繋がり、「海外に留学しなくても、ここにいれば世界最先端の研究ができる」阪大心臓血管外科のブランドを築き上げた秘訣なのだろうと感じました。
(インタビュアー・執筆 早川威士)
(ASCA Bulletin 21号 2018年12月発行より)
ASCA Bulletinとは:
アスカコーポレーションが年3回発行している広報誌です。ご興味のある方は、弊社営業部までご連絡ください。


